中国细胞与基因治疗产业发展白皮书 细胞技术研发与应用的新纪元
引言
随着生物科技的飞速进步,细胞与基因治疗(CGT)作为现代医学的革命性前沿,正引领着全球医疗健康产业的深刻变革。在中国,得益于国家政策的强力支持、资本市场的持续投入以及科研实力的稳步提升,细胞与基因治疗产业已进入快速发展阶段,尤其在细胞技术的研发与应用领域展现出巨大潜力与独特优势。本白皮书旨在梳理中国细胞与基因治疗产业的发展现状,重点聚焦细胞技术的研发进展与临床应用,并展望其未来趋势与挑战。
一、产业发展背景与政策环境
中国已将生物经济列为国家战略性新兴产业,细胞与基因治疗是其中的关键支柱。《“十四五”生物经济发展规划》等纲领性文件明确提出了加快发展细胞治疗、基因治疗等前沿技术的要求。国家药品监督管理局(NMPA)近年来加速了相关技术评价指南的出台与完善,为CAR-T、干细胞等产品的临床研究和上市审批建立了更为清晰、科学的监管路径。地方政府也纷纷出台配套政策,建立产业园区,形成了一批如上海、北京、深圳、苏州等具有国际竞争力的产业集群。稳定的政策预期和逐步完善的监管体系,为产业的创新研发与商业化应用提供了坚实基础。
二、细胞技术研发进展
在细胞技术研发层面,中国已从早期的跟跑逐步实现并跑,并在部分领域展现出领跑潜力。
- 免疫细胞治疗:以嵌合抗原受体T细胞(CAR-T)为代表的免疫细胞治疗是当前最成熟的领域。国内企业自主研发的CAR-T产品已有多款获批上市,用于治疗复发/难治性血液肿瘤,疗效显著。研发重点正从血液肿瘤拓展至实体瘤,并通过开发通用型CAR-T、双靶点CAR-T、CAR-NK等新技术,致力于解决现有疗法的持久性、安全性与可及性问题。
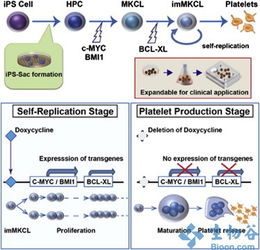
- 干细胞治疗:在间充质干细胞(MSCs)、诱导多能干细胞(iPSCs)等领域基础研究与临床转化并进。MSCs在骨关节疾病、移植物抗宿主病(GVHD)、自身免疫性疾病等方面的临床研究广泛开展。iPSCs技术为疾病建模、药物筛选和再生医学提供了无限细胞来源,其在帕金森病、年龄相关性黄斑变性等领域的临床研究已进入早期阶段。
- 其他新型细胞技术:肿瘤浸润淋巴细胞(TIL)疗法、T细胞受体(TCR-T)疗法、干细胞衍生细胞产品(如胰岛细胞治疗糖尿病)等也处于积极的研发管线中,技术路线呈现多元化、精准化发展趋势。
三、细胞技术的应用与临床转化
研发的最终目标是惠及患者,临床应用是检验技术价值的核心标尺。
- 血液肿瘤治疗:CAR-T疗法已成为部分白血病、淋巴瘤患者的“救命疗法”,填补了临床空白,显著提升了患者的生存希望与生活质量。
- 实体瘤挑战与突破:针对肝癌、胃癌、脑胶质瘤等实体瘤的细胞治疗临床试验正在广泛开展。克服肿瘤微环境抑制、提高细胞浸润能力、寻找更优靶点是当前应用攻关的重点。
- 再生医学与罕见病:干细胞疗法在脊髓损伤、骨软骨缺损、心血管修复等再生医学领域展现出修复潜力。基因修饰的干细胞疗法也为一些遗传性罕见病(如地中海贫血、免疫缺陷症)提供了根治性希望。
- 临床应用生态:国内领先的医院与研发企业紧密合作,建立了从细胞采集、制备、质量检测到回输治疗的标准化临床操作与管理体系,为技术的安全有效应用保驾护航。
四、面临的挑战
尽管前景广阔,产业发展仍面临诸多挑战:
- 技术瓶颈:如实体瘤疗效有限、治疗副作用(细胞因子释放综合征等)的管理、制造成本高昂、长期安全性数据仍需积累等。
- 可及性问题:目前上市产品价格昂贵,医保覆盖有限,普通患者经济负担重。简化工艺、降低成本、探索多元化的支付方式是当务之急。
- 供应链与标准化:细胞产品的个性化特性对冷链物流、全程追溯、质量控制提出了极高要求,建立稳定、高效、标准的供应链体系至关重要。
- 伦理与规范:随着基因编辑等技术的应用,相关的伦理审查、知情同意、数据隐私保护等社会伦理与法规问题需持续关注与规范。
五、未来展望与建议
中国细胞与基因治疗产业将在创新、合作、规范中迈向新高度。
- 强化源头创新:鼓励面向临床需求的底层技术(如新型基因编辑工具、递送系统、细胞工程化技术)和前沿交叉学科(如合成生物学、人工智能辅助设计)的原始创新。
- 完善生态体系:推动“产学研医资”深度融合,加强临床研究能力建设,优化审评审批流程,加速产品上市。积极探索商业保险、专项基金等创新支付模式。
- 推动国际化:鼓励国内企业参与国际研发与合作,推动中国创新的细胞治疗产品走向全球市场,贡献中国智慧与方案。
- 坚守安全与伦理底线:在鼓励创新的建立健全全生命周期的监管与伦理框架,确保产业在安全、合规的轨道上健康发展。
###
中国细胞与基因治疗产业,特别是细胞技术领域,正站在从技术突破迈向大规模产业化应用的关键历史节点。通过持续的技术研发、理性的临床探索、完善的生态构建与审慎的监管护航,中国有望在全球这一尖端科技与产业竞争中占据重要一席,最终为攻克重大疾病、提升人类健康福祉做出决定性贡献。
如若转载,请注明出处:http://www.cyagencellservice.com/product/53.html
更新时间:2026-05-21 09:42:22